以GLP-1靶点为代表的药物,因其减肥功效正在成为资本市场的“新宠”。
此前,特斯拉首席执行官埃隆·马斯克亲自试药“司美格鲁肽”,令诺和诺德、礼来等老牌GLP-1研发药企备受关注,截至12日16时收盘,诺和诺德在纽交所的最新股价已达100.18美元,市值超4479亿美元。13日A股盘中,受隔夜美股诺和诺德、礼来走势提振,博瑞医药、百花医药、众生药业等个股纷纷涨停,翰宇药业、昊帆生物、乐普医疗等涨幅居前,这些药企均有业务涉及GLP-1药物的研发、生产与服务。
事实上,诺和诺德、礼来几乎已瓜分了全球GLP-1大部分的市场份额,作为追赶者,国内一众药企面临着怎样的竞争格局,是否可以实现弯道超车?
受减肥市场带动
市场看好GLP-1的核心逻辑何在?
“GLP-1是一个非常成熟的靶点,很早就被用于糖尿病治疗药物的开发,但资本市场对于该靶点相关药企的投入,主要还是因为看好减肥减重这一赛道,也就是说,它兼具了医疗和消费的属性。”金浦健康基金合伙人缪宇在接受第一财经采访时表示,GLP-1的市场规模也在一定程度上给到机构参与者更多的信心。
从全球情况来看,《经济学人》报道称,预计2031年全球GLP-1类药物整体销售规模有望达1650亿美元规模。摩根大通分析师也于近日表示,预计2030年全球GLP-1药物市场年销售额将超过1000亿美元。
从国内情况来看,西南证券在今年9月发布的一份报告称,参考PDB样本医院放大版数据,2022年我国GLP-1RA市场规模约60.5亿元,2018至2022年的复合年均增长率达70.5%。
GLP-1于1987年被发现,是血糖稳态调节的重要靶点;而GLP-1RA则被研发用于改善2型糖尿病的一些关键性病理生理缺陷,并具有减少心血管死亡、改善动脉粥样硬化、减轻体质量、降低收缩压等降糖外的获益。
由于天然GLP-1的半衰期极短,因此,GLP-1RA的发展经历了从短效到长效再到超长效的过程。现阶段,国内获批上市的短效GLP-1RA包括艾塞那肽、贝那鲁肽、利司那肽,长效GLP-1RA包括利拉鲁肽,而超长效GLP-1RA则包括司美格鲁肽、度拉糖肽、聚乙二醇洛塞那肽等。
“司美格鲁肽、利拉鲁肽等此前做的适应证是2型糖尿病,但由于患者每天要往肚子上扎针,并且国际指南提到可以将其作为联用药物,因此依从性并不高。而自从司美格鲁肽在美国获批了减重适应证后,市场销售一度有了很大提升。”缪宇说。
国内相关药物研发及上市进展如何?第一财经记者梳理相关数据发现,华东医药一款用于减重适应证的利拉鲁肽已于7月获批上市,其他正在开展GLP-1RA不同阶段临床试验的主流药企数量超过20家。
其中,超长效产品用于肥胖适应证上,信达生物、先为达生物、鸿运华宁、银诺医药均有多肽或单抗类产品正处于III期临床试验阶段,博瑞医药的BGM0504、恒瑞医药HRS9531则处于Ⅱ期临床试验,这还不包括短效、超短效产品。礼来、诺和诺德则均有口服用于肥胖适应证的产品进入III期临床试验。
“国内来看,肥胖适应症方面还没有超长效产品上市。”缪宇说,一方面,患者对于口服产品的依从性会比注射剂更好,另一方面,司美格鲁肽一类产品在国内是纳入医保范畴的,价格也不高在478元/支,“因此,GLP-1RA产品未来必定会面临白热化的竞争格局。”
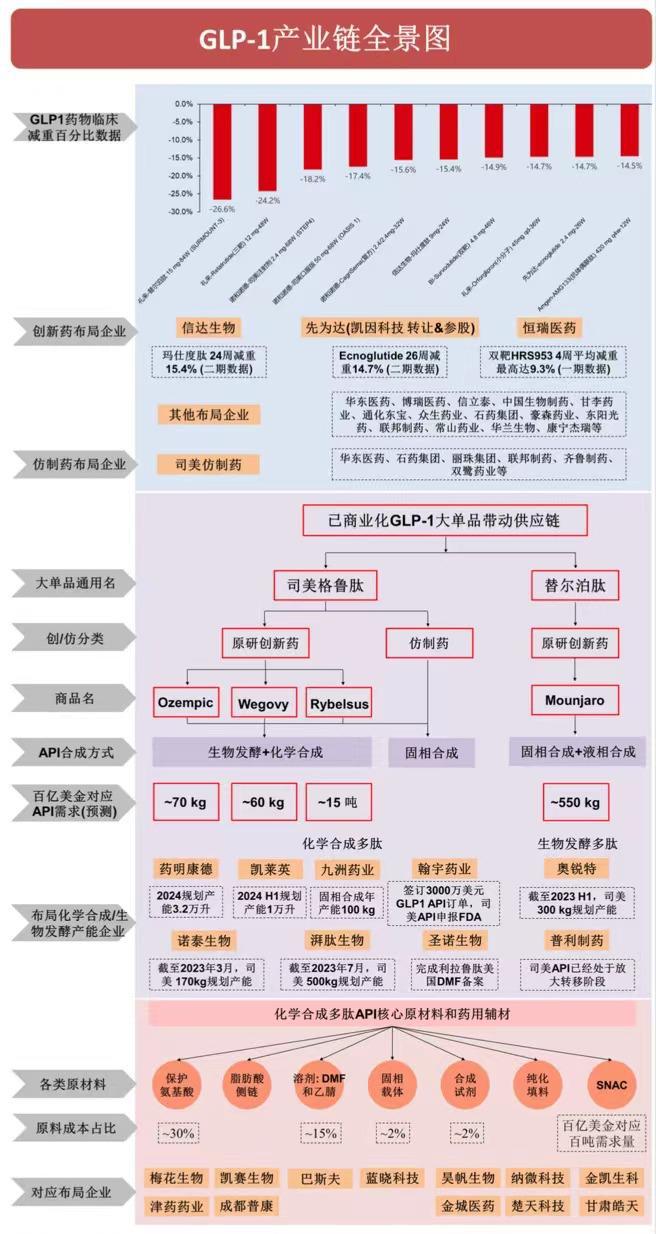
(GLP-1产业链全景图。来源:中信证券研报。)
而睿郡资产首席研究员魏志华则表示,会持续看好GLP-1RA在减肥市场的布局,包括相关药物在一些新的、大的适应证的拓展,包括NASH、AD等,但也会关注GLP-1RA的上游原材料产业包括多肽、药用辅材等领域的企业,“国内药企竞争激烈是一定的,但最终还是要看临床进展的快慢,以及临床数据的优劣。”
临床风险需重视
实际上,使用司美格鲁肽等GLP-1RA也被指出会引起恶心、反胃、肠梗阻和胰腺炎等副作用和不良反应;那么,相关临床风险如何看待,怎样避免?
为此,上述两位投资人士称,一方面,司美格鲁肽在全球范围内已是一个相对成熟的产品,也积累了大量真实世界的数据,安全性有所保证;另一方面,每个药物都或多或少有副作用,也是看不良反应发生概率的大小,这也是药物是否能过审上市的关键,但对于后续药企进行迭代产品的开发上,则建议专注在提高疗效、降低副作用等方向进行不断优化及改进。
临床如何应对上述风险?记者了解到,一份由中华医学会于2021年4月发布的《中国2型糖尿病防治指南》中提到,单独使用二甲双胍治疗血糖仍未达标,则可使用GLP-1RA进行二联治疗。
另一份由广东省药学会于2023年4月发布的《GLP-1RA临床应用医药专家共识》则在“药效评估”部分指出,“在患者使用GLP-1RA治疗期间不仅要监测血糖和糖化血红蛋白,判断是否需要增加/减少用药剂量,或者联用/减少其他降糖药物;还要监测血压、血脂,判断是否需要联用降压、降脂药物;对于肥胖的患者,要监测体质量指数,在可耐受的情况下逐渐增加到GLP-1RA的最大剂量”。
该《共识》称,国内批准上市的GPP-1RA的药品说明书适应证,均为单用/联用二甲双胍、磺酰脲类口服降糖药疗效不佳的成人2型糖尿病患者的血糖控制;《共识》同时罗列了包括胃肠道反应、低血糖、超敏反应、心率加快、急性肾损害、胆石症和胆囊炎等多种不良反应的监测和处理方法。
为此,广东省药学会药物治疗管理专业委员会主任委员曾英彤表示,司美格鲁肽和利拉鲁肽在国外获批了获批减重的适应证,并可每周1次皮下注射2.4mg用于减重,但其“用于减重的剂量比用于降糖的剂量更大”。
曾英彤强调,在国内,一些GLP-1RA药物在减肥减重上的适应证并未获批准,如果是临床使用GLP-1RA进行减肥减重的,则需要遵循医院的超说明书用药的管理制度和流程。
“目前,我院还没有相关用来减肥减重的GLP-1RA药物可以为患者开具类似处方。对于GLP-1RA药物的使用,也是严格遵循国内指南来进行。”上海一家三甲医院内分泌临床医生告诉记者,一些医院开设了减重门诊,这些门诊是专门针对患有肥胖疾病的人群,为他们提供治疗方案。
该医生也表示,从GLP-1药物的说明书或文献列举情况来看,其可能会产生的不良反应种类远不止上述《共识》中所罗列的,对于单纯想要变瘦的个人来说不建议擅自购买使用,“不良反应发生率不高通常对应的是人群概念,但从个人来讲,只有0和1的区别。超说明书用药有着不确定性,这也是很多医院不会给患者开药用于减肥的原因。”
本文内容由互联网用户自发贡献,该文观点仅代表作者本人。如发现本站有涉嫌抄袭侵权/违法违规的内容,请发送邮件至 3587015498@qq.com 举报,一经查实,本站将立刻删除。本文链接:https://www.xmnhj.com/h/265915.html

