
中国基金报记者 米洛 卢鸰
9月15日,有网络传闻称,“恒瑞子公司瑞石生物宣布解散,瑞石现场产生冲突。”
恒瑞知情人士向记者透露:“瑞石生物的情况具体怎样还需要等公司官方信息。但瑞石生物体量不大,仅百来名员工,对公司来说影响有限。另外,SHR0302强直性脊柱炎NDA申请刚获受理,其他适应症研发仍在正常进行,估计不会受到影响。”
凭借着明星产品和“药茅”恒瑞背景,瑞石生物一直被视为生物制药创业明星。就在去年5月,有机构宣布,参与了瑞石生物近1亿美元A股融资。
去年获近1亿美元融资
背靠恒瑞医药,瑞石生物一直被视为明星创业公司。
资料显示,瑞石生物是一家临床阶段的生物制药公司,致力于研发创新药物,专注于具有未被满足临床需求的免疫炎症性疾病。

资料显示,瑞石生物由恒瑞医药在2018年初孵化共同成立,始终定位在立足中国、放眼全球,成立以来汇聚业界顶尖人才,深耕免疫炎症的新药研发,聚焦于炎症性消化、皮肤、神经等自身免疫疾病领域,全球多中心临床试验和新药研发齐头并进。
另据公开报道,2019年11月,恒瑞医药全资子公司盛迪医药收购香港瑞石医药95%股份项目获得备案,投资总金额为9500万美元。
彼时,恒瑞医药董事长孙飘扬表示:“我们很高兴能够投资瑞石。相信在王敏博士及其管理团队的努力下,恒瑞的中国原创药一定能成功地进入欧美国家。同时瑞石发挥其优秀的全球临床开发能力,与更多的合作伙伴一起成功地为全球及中国患者带来更多创新治疗药物。”
2022年5月,瑞石生物又完成了近一亿美元A轮融资。
公开报道显示,这轮融资由华盖资本旗下医疗基金及其管理的首都大健康基金共同领投,楹联健康基金、张江浩、清科产投、翰颐资本跟投。
重磅新药上市许可申请获受理
对目前市值约为2800亿元的恒瑞医药来说,手握重磅新药的瑞石生物颇为重要。
早在2018年10月,恒瑞医药就披露过瑞石生物的研发进展。
彼时,恒瑞医药表示,瑞石生物在2018年9月17日向美国食品药品监督管理局提交了SHR0302片临床试验申请并获受理。

公司表示,SHR0302片的同类产品有辉瑞公司开发的托法替尼。托法替尼最早于2012年11月在美国获批上市,最初获批用于类风湿性关节炎治疗,2018年5月获批用于溃疡性结肠炎治疗,是目前唯一批准用于溃疡性结肠炎治疗的 JAK 激酶抑制剂,该药品已于 2017 年 3 月在国内获批上市。
2017年托法替尼全球销售额约为14.57亿美元。
此后,恒瑞医药一直在公告中披露SHR0302片的进展。
今年8月,恒瑞医药公告称,公司提交的SHR0302片药品上市许可申请获得国家药监局受理。
此次,恒瑞医药透露,2022年托法替布片和乌帕替尼缓释片全球销售额合计约为42.78亿美元。
截至发布公告时,SHR0302相关项目累计已投入研发费用约7.62亿元。
从高管任职来看,恒瑞医药对瑞石生物颇为重视。
孙飘扬自2018年4月开始担任瑞石生物的董事长,恒瑞医药董事、副总经理张连山也在瑞石生物担任董事。
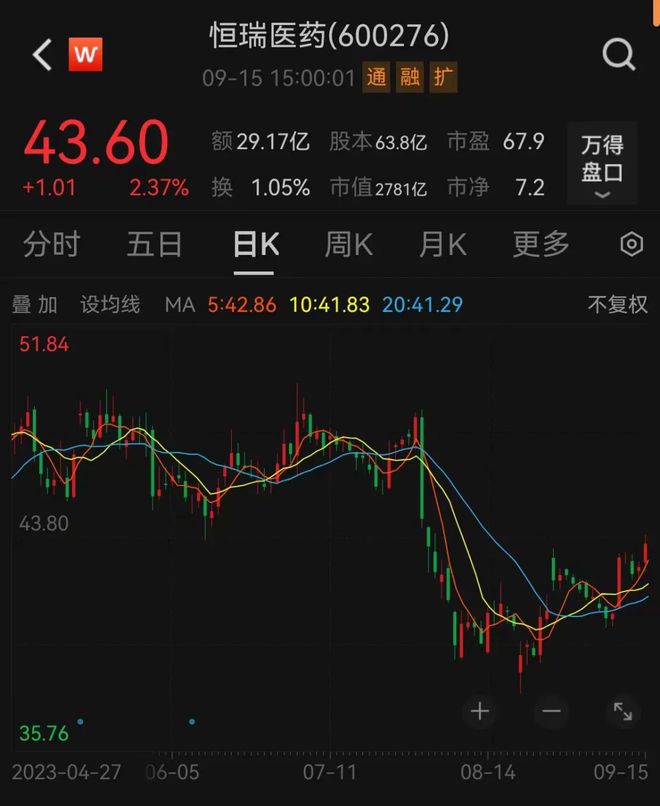
截至9月15日,恒瑞医药股价43.60元,市值2781亿元。
编辑:舰长
审核:许闻
版权声明
《中国基金报》对本平台所刊载的原创内容享有著作权,未经授权禁止转载,否则将追究法律责任。
授权转载合作联系人:于先生
本文内容由互联网用户自发贡献,该文观点仅代表作者本人。如发现本站有涉嫌抄袭侵权/违法违规的内容,请发送邮件至 3587015498@qq.com 举报,一经查实,本站将立刻删除。本文链接:https://www.xmnhj.com/h/230544.html

