
没人能否认License in模式的精妙之处,但不得不说,对于药企而言,这一模式考验重重。
不仅考验药企的眼光、临床能力,更考验心理素质和创新信仰。毕竟,一种极端情况是,药物海外临床率先遭遇滑铁卢。
海外临床失败,并非都是药物出现了问题,也有可能是临床设计不合格。
退一万步而言,即便是药物本身不行,但只要层层分析数据,或许依然能够找出优效人群,索元生物的商业化模式就是如此。
对于药企而言,面对这种情况,如何抉择是一个不小的考验。
一旦并非药物临床的问题,那么对于药企来说,只有两条路可选:
要么放弃现有投入转战其它管线,要么通过更为“巧妙”的临床设计,以获得更好的临床结果支撑药企预期。
从药企经营角度来说,做出任何一种选择都有可能,这无关对错。但从医药行业的发展来说,毅然选择前者的药企越多,说明中国医药行业的改革越成功。
撕下低端药品倾销地标签
2015年以前,中国市场一度被海外媒体称为低端药品的倾销地。因为,彼时一些在海外因疗效未能获批上市的药品,却能在国内获得新生。
比如,疫情期间为人熟知“神药”日达仙。这是由美国赛生药业生产的一种胸腺肽注射剂,面世之初,赛生药业对日达仙的研究集中于肝炎和肿瘤,这两大市场规模最为庞大的领域。但在这些领域,日达仙并没有证明自己。
2005年12月,赛生药业宣布,根据一项三期临床数据,没有证据显示日达仙对治疗丙肝患者有所帮助。而在肿瘤治疗领域,也没有证据表明它可以提高对抗肿瘤治疗的反应率。
这导致,日达仙在国外大部分国家,都难以上市销售,销路一直难以打开。但在国内,日达仙获准用于治疗丙肝和作为疫苗佐剂,一些肿瘤科也使用日达仙辅助治疗。2005年,日达仙全球销售额回升至2780万美元,其中约2500万美元自中国。
这类药物之所以能够在国内上市,某种程度上是特殊时代的产物。
当时,在郑筱萸主导下的创新药发展几乎停滞,药品审批注册成为一件花钱就能办的事情,且药品临床试验数据大量造假,导致大量劣质、无效药通过审批进入市场。
但2015年后,“722”事件发生,整个行业开始自查核查临床试验数据,低效、无效药物再难以进入中国市场。
加之开启一系列政策改革,中国创新药大发展的时代序幕就此拉开。
中国创新药企开始以一个更高、更严的评价标准要求自己,出海证明自己也成为众多药企的共同追求,监管机构的的审批标准也向严苛的FDA靠近。
经过数年间的不断发展,如今的中国早已撕下低质量药物倾销地的标签。
海外临床失败的药物还能在国内上市吗?
最近的一则消息,又唤起了医药人对那个混乱时代的记忆。
4月25日,天麦生物引进的口服胰岛素ORMD-0801在国内的上市申请获得NMPA受理。
在全球范围内都没有口服胰岛素成功的先例,如果ORMD-0801能够获批上市,将成为全球首个口服胰岛素。
这本该是喜事一桩,然而一些业内人士却难言喜悦。因为就在三个月之前,这款药物的海外III期临床试验失败了。
1月12日,以色列药企Oramed宣布,在为期26周的临床试验中,ORMD-0801在改善血糖控制方面的效果还不如安慰剂。鉴于这一结果,Oramed表示将停止ORMD-0801用于2型糖尿病的适应症研发,未来基本也不会再开发口服胰岛素。
而根据《药物临床试验登记与信息公示平台》显示,目前国内ORMD-0801治疗2型糖尿病的III期试验已完成。
同样一款药物,国内外却做出了不同的效果,这自然也引起了不少人的好奇。在部分市场人士看来,这款药物在国内的成功或许是因为临床试验的“取巧”。
事实上,通过对比可以看到,ORMD-0801在海内外进行的两项临床试验标准并不相同。
首先,从入组人数上来说,国内临床试验入组522人,国外临床试验入组710人。从统计学来看,样本量越小,研究结果越不稳定,得到“假阴性”错误结果的风险也大。当然,人数的差异并不足以如此显著地影响临床试验的结果。
更重要的是,国内外临床试验患者入组的标准并不一样。
国内入组需要患者对1~2种口服降糖药治疗疗效不佳,患者的BMI在18.5~30 kg/m2。海外临床试验中则需要患者接受过2~3种口服降糖药治疗,患者BMI为 25-40 kg/m2。
BMI是目前判断是否超重及肥胖最常用的一个临床指标,这一数字越大,患者的肥胖程度也就越严重。而随着肥胖患者体重的增加,2型糖尿病病情也会加重。
简单来说,国外试验患者的糖尿病病情,大概率要比国内患者病情更严重。一定程度上,入组患者情况越好,试验也就更容易做出效果。
其次,两个试验的用药剂量也并不相同。国内患者用药剂量更高,为每日三次,每次16mg。而在海外,则使用了8mg的剂量,每晚服用一次。更大的药物剂量或许是希望大力出奇迹。
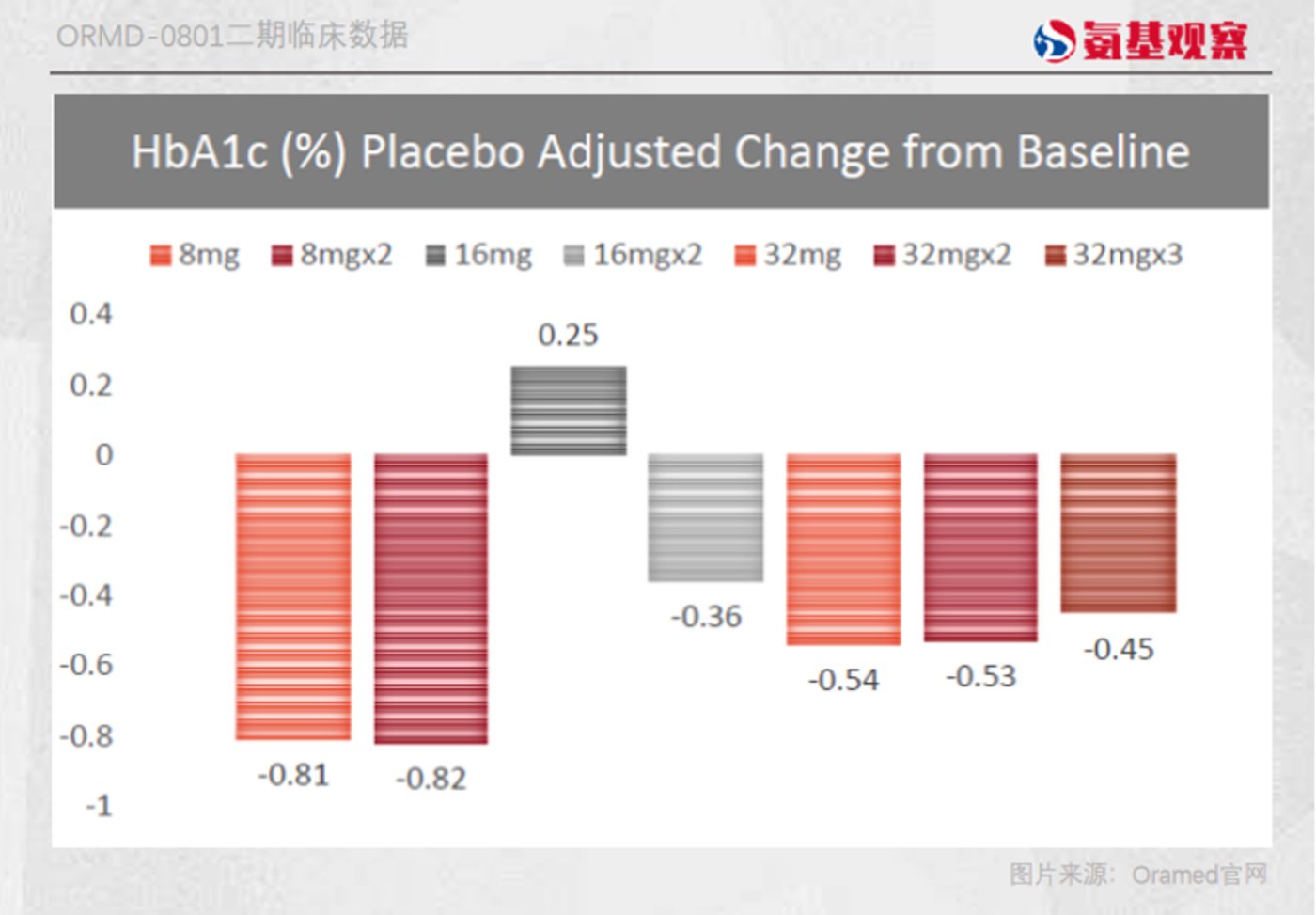
然而根据Oramed此前公布二期临床数据显示,ORMD-0801在临床实验中出现了量效关系倒挂,在8mg时ORMD-0801降糖效果最好,随着剂量提升ORMD-0801降糖效果反而出现了下降。
那么,在这种情况下,天麦生物为何仍选择高剂量用药,我们不得而知。ORMD-0801的具体临床数据并未披露,这款药物到底是因为临床试验“投机取巧”获得成功,还是因为人种差异使得其对国人有“特效”,答案也未可知。
不过,我们希望,答案会是后者。
中国创新药发展不能开倒车
如今,在海外临床试验失败的药物,在国内也难以通过监管的批准。
比如,万春医药的普那布林。FDA认为一个三期注册临床不能充分证明普那布林治疗获益,要求进行第二项注册临床,所以未批准普那布林上市。而在国内,普那布林的上市申请,同样未获NMPA的批准。
ORMD-0801能否在国内获批上市,答案还未可知。至于海外临床失败的药物能否国内上市这一问题,索元生物或许更急迫想要证明,能。
因为其核心商业模式是,直接收购或引进后期临床试验失败的管线,媒体称之为“死药重生”。
按索元生物的说法,虽然药物临床失败,但通过对临床数据的仔细分析,或许还能找到获益的特定人群。基于这一人群的特征,再去寻找相应标志物,开发first-in-class产品,不仅成本低、时间短,成功率还高不少。
关于这一模式,索元生物还表示,“利用生物标志物进行药物再开发已有易瑞沙、奥拉帕利等案例,而采用更换适应症等方式进行药物再开发的则更普遍,知名案例包括新基制药的来那度胺再开发案例等。”
的确,模式并无问题,但一切的一切还要靠实际临床数据说话,而非投机取巧。
毕竟,如今的中国创新药经历了数年的发展,才换来今日之局面。
早些年,有益于中国由于缺医少药,且创新药政策也并不完善,迫切需要解决从无到有的问题,所以一些me too乃至me worse药物,也就有机会上市。
当时,这种模式为国内输送了大量国外药物,也满足了临床用药基本需求。但现阶段,中国的创新药事业已经阶段性完成由少到多、由小到大的蜕变,接下来的目标是实现由大到强。
事实上,随着我国创新研发水平的逐渐提高和前期的技术、资金积累,已经有越来越多的药物,在最为严苛的美国市场受到了认可,比如百济神州的泽布替尼、传奇生物的CARVYKTI。
当然,与全球市场相比,我们的创新药物仍不够多,这必然需要,国内药企们继续以海外的优秀药物为标杆,以更为严苛临床试验标准要求自己,推动创新药不断向上发展。
而那些为了药物能够成功上市,进行“投机取巧”式临床试验的行为,是断不可取的。因为,中国创新药发展不能开倒车。
过去几年里,中国创新药取得了巨大的进步,这离不开每一个医药人的努力。
未来,中国创新药这艘巨轮的前进方向,仍然握在所有医药人手中,只有每一个医药人都选择前进,巨轮才能乘风远航。
本文内容由互联网用户自发贡献,该文观点仅代表作者本人。如发现本站有涉嫌抄袭侵权/违法违规的内容,请发送邮件至 3587015498@qq.com 举报,一经查实,本站将立刻删除。本文链接:https://www.xmnhj.com/h/159599.html

